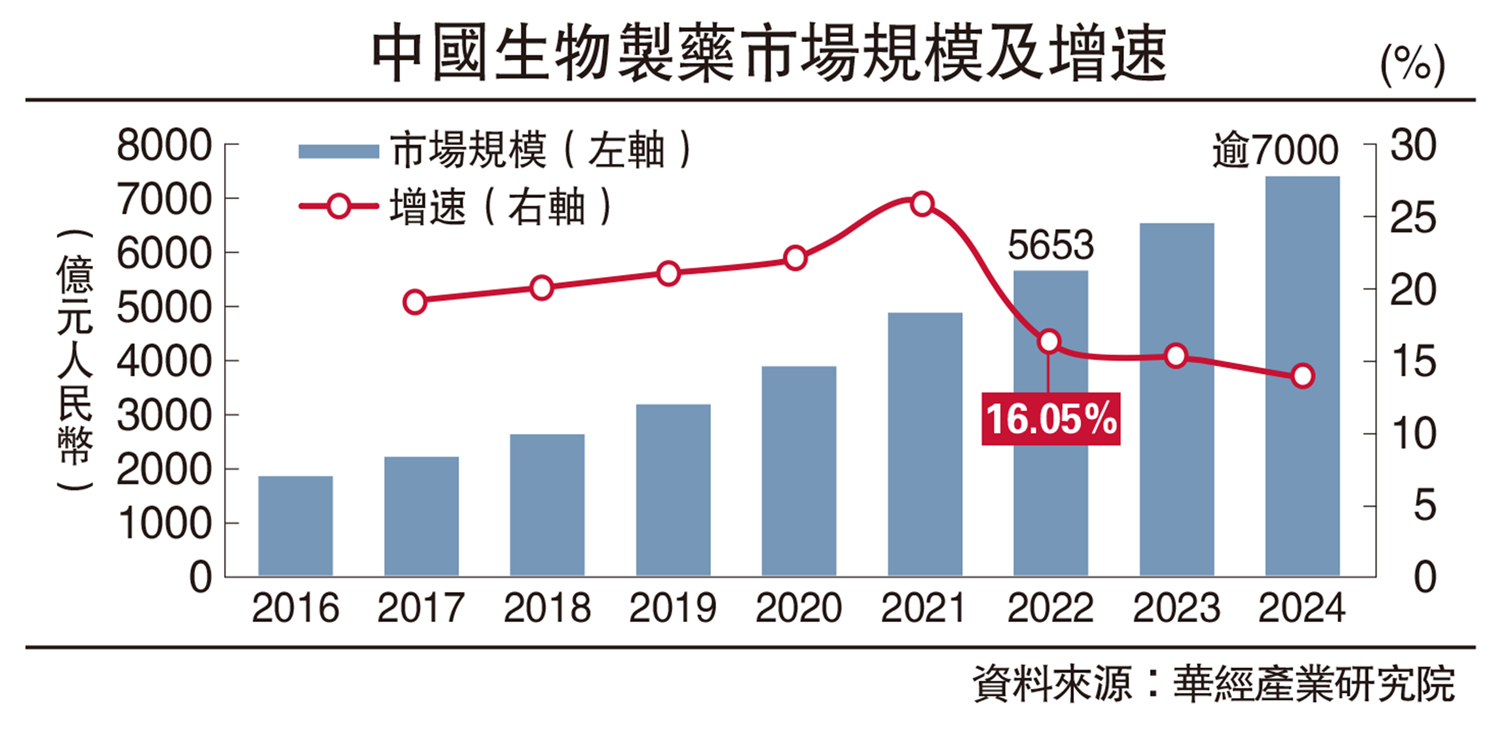
中央政府日前公布了「十五五」規劃建議,為國家經濟和社會發展制定中長期藍圖,各行各業均可從中一窺未來發展方向。作為一個長期深耕醫療健康的投資人,筆者很高興看到「十五五」再次明確「支持創新藥和醫療器械發展」,並第一次將生物製造、腦機界面等列入前瞻布局的未來產業,為生物科技和醫療藥械發展帶來巨大機遇。
規劃提出,要加強原始創新和關鍵核心技術攻關,採取超常規措施,推動積體電路、工業母機、高端儀器、基礎軟體、先進材料、生物製造等重點領域,關鍵核心技術攻關取得決定性突破,以加快高水準科技自立自強,引領發展新質生產力。同時,規劃提出實施健康優先發展戰略,支持創新藥和醫療器械發展、全方位勾勒出以人民健康為中心的民生保障藍圖。
生物醫藥產業被定位為「新質生產力」的核心領域,官方明確將通過完善政策支持、金融支持和數據應用等,為行業發展提供系統性支持,例如通過研發費用加計扣除、稅收優惠等激勵措施,引導企業加大原始創新投入,並將「AI+醫療」等技術深度融入產業。國家發改委、科技部、藥監局等部委也聯合出台多項支持政策。
各省政府也將生物醫藥納入重點發展規劃,通過專項基金、人才引進計劃等手段,將國家戰略轉化為區域發展動能,形成「中央統籌+地方特色」的協同格局。那麼,在「十五五」規劃中獲支持建設「國際創新科技中心」的香港,又該如何乘勢突破?
香港作為超級聯繫人、超級增值人,除了通過本港平台可協助內地的生物醫藥企業「走出去」拓展國際業務,也不斷將海外相關企業「引進來」,對接本港和內地企業共拓商機。近年特區政府正大力推動本港成為國際醫療創新樞紐,一方面積極改革藥械審批制度,另一方面加強生物醫藥技術研發轉化,為生物醫藥企業創造有利的營商環境,同時協同粵澳推進大灣區科技創新合作,當中包括助力生物醫藥等科技產業升級發展。
近期值得業界關注的發展之一,是香港和深圳以「一河兩岸」、「一區兩園」理念共同構建的河套合作區。河套香港園區處於特殊的地理位置,也獲得專屬的創新便利措施支持,生物醫藥產業是區內其中一項重點發展產業。國家積極擴大內地科研數據跨境至河套香港園區供區內企業機構使用,並有機會允許生物樣本通過合作區跨境流通,對進一步吸引更多海內外企業落戶香港,或加大在香港的投資規模起正面作用。
今年的施政報告中特別提到,將透過河套的「大灣區臨床試驗協作平台」,讓藥企在港深同步開展試驗。同時籌備成立「國際臨床試驗學院」,培育大灣區臨床試驗人才,以及舉辦國際高峰會議和論壇等。目標是吸引更多藥企落戶香港,進行罕見病藥、高端腫瘤藥及先進療法製品等臨床試驗和治療,同時也會推動大灣區內臨床數據標準化,構建真實世界數據平台,助力藥企更快將創新藥物推向內地和國際市場。再加上,香港擁有良好的貿易網絡、獲國際認可的醫療系統和臨床試驗平台,配以豐富的金融資源,可以預期大灣區的生物醫藥產業將迎來新一輪的合作發展機遇。
港簡化藥品註冊上市過程
此外,香港於2023年11月推出新藥審批機制「1+」,簡化內地和海外的藥品註冊上市過程,便利來自內地及各地符合本地醫療需要的新藥來港註冊。隨着香港註冊用藥使用「1+」機制上市,可幫助更多內地創新藥先行落地在香港使用,然後進一步利用在香港上市的往績拓展海外市場。截至2025年9月初,共有14款新藥按此機制獲批准註冊。政府更表明會加快「1+」新藥審批機制,並試行優先審批經醫院管理局建議能應對治療嚴重或罕見病的創新藥,助力藥企更快將創新藥推向市場。
最令人期待的是繼衞生署今年6月正式公布「香港藥物及醫療器械監督管理中心」(簡稱CMPR)成立時間表及新藥「第一層審批」路線圖,今年施政報告中亦提到會於2026年內成立CMPR,並提交規管醫療器械的立法建議,力爭到2030年全面實現新藥械的自行審批。CMPR的成立,不僅是香港打造國際醫療創新樞紐的關鍵一步,也將對內地藥械行業產生深遠而積極的影響。
因為CMPR實施的「第一層審批」機制,其主要功能與職責涵蓋制定法規標準、開展註冊審批、實施上市後監管、促進產業發展和加強國際合作等範疇,將為內地創新藥械開闢更為便捷的註冊通道,加速其成功進入香港市場。憑藉香港作為高度國際化市場的優勢,其認可將有力助推內地藥械產品走向更廣闊的國際舞台,同時能夠進一步反哺中國藥品監管水準,打造與世界同步的藥品監管體系。
屆時無論是國內外企業都可考慮利用香港的優勢,配合國家自主研發創新藥的崛起,積極拓展香港和大灣區業務,提升規模和競爭力,並透過專利授權開拓國際市場,為香港帶來極大經濟和戰略機遇。
(作者為創業投資者聯盟召集人)