創科宇宙/中國創新藥警惕出海挑戰\梁頴宇
「出海」是中國生物醫藥企業近年一個重要課題,尤其在創新藥領域,由創新藥BD(商業拓展)催化的出海熱,正從個別企業的嘗試,演變為行業集體的戰略共識。但面對瞬息萬變的環境,藥企積極「走出去」的同時,也要認識到當前出海模式存在的局限,警惕產業鏈外遷風險與國際科技競爭帶來的挑戰。
中國藥企憑藉多年持續的研發投入,創新成果近年取得突破,成了跨國藥企管線補給站,以對外授權為主的BD交易連年上升。2025年,創新藥對外授權交易總額攀升至逾1356億美元,佔全球交易總額49%,超越美國成為全球創新藥對外授權第一大市場。今年以來,醫藥上市公司BD交易金額與首付款持續刷新紀錄,如石藥集團與阿斯利康的185億美元戰略合作。
跨國藥企搶購中國創新藥,藥企通過創新藥「授權出海」融入全球體系,在世界舞台扮演越來越重要的角色,固然是值得高興的進展;但是近期石藥集團在大額授權消息公布後,股價不升反跌,部分企業亦因大額授權而導致估值下跌,折射出資本市場對「賣青苗」模式的負面效應加劇,是一個不可忽視的信號。
之前BD交易能催化藥企的股價,主因是內地生物科技和醫藥領域經歷了幾年寒冬,不少藥企的估值與業績預期被嚴重低估;而一筆重磅BD交易不僅能提供短期現金流支持產品後續研發,並提升產品認受性,交易金額甚至可能超過企業當時的總市值。
但大批創新藥「授權出海」的背後,一個不爭現實是國內市場利潤空間持續收縮,創新藥商業化回報不足,特別是醫保控費、集採常態化使創新藥上市後的價格快速下探,難以覆蓋高額研發投入。加上熱門賽道集中度高、同質化競爭嚴重,藥企在國內難以形成穩定現金流,出海也可能是一個不得已的選擇。
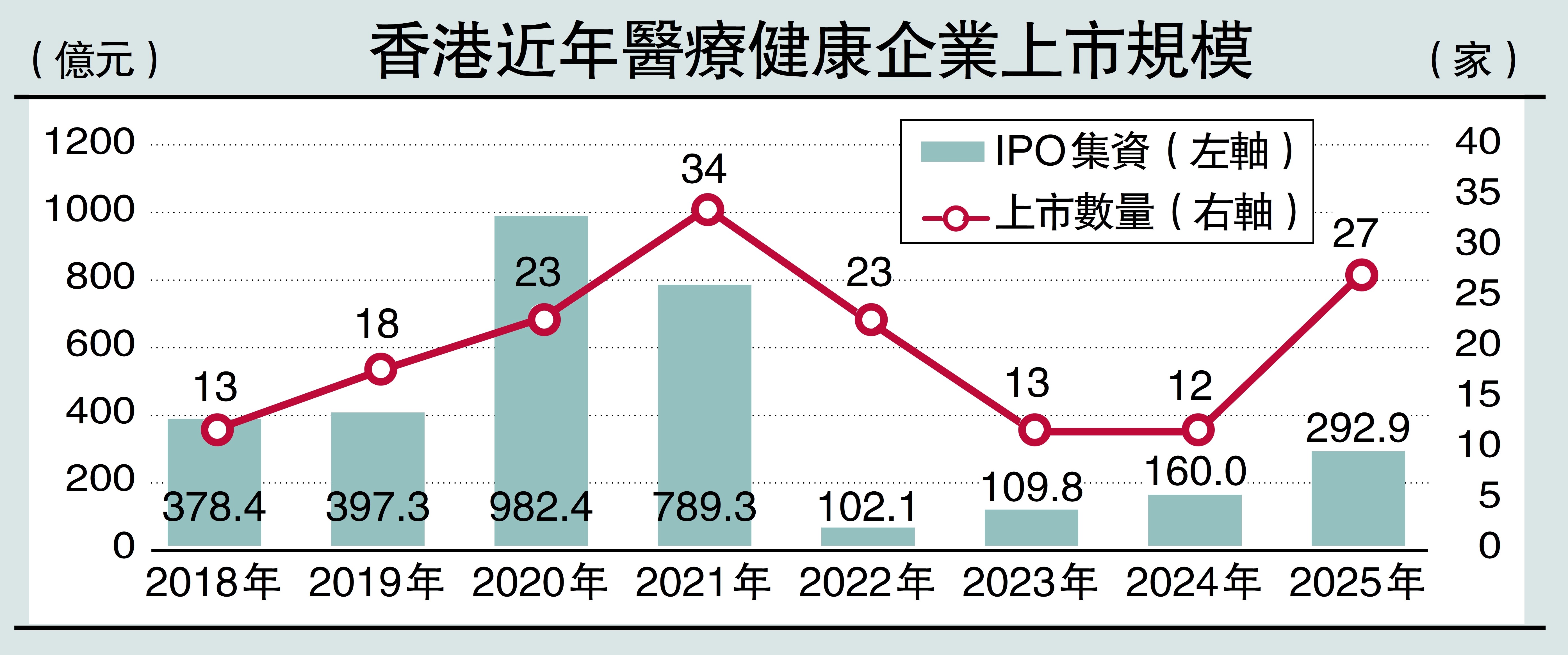
隨着去年IPO市場回暖,上市融資之路重啟,2025年共有41家醫療健康企業成功發行IPO,募資總額超過396億元(人民幣,下同)。資本市場開始出現「賣青苗焦慮」,由之前擔憂藥企能否生存,變成害怕長期依賴對外授權交易會導致核心資產過早外流,長期商業化收益被讓渡。長遠來看,還可能導致全球化能力建設不足,難以形成自主商業化體系。若繼續依賴對外授權交易,中國創新藥將長期停留在全球價值鏈低端。
因應中國創新藥全球認可度提升,國際資本與跨國藥企加大對中國企業和人才的吸引力度,而由於國際資本更偏好「海外資產+全球權益」模式,中國企業在海外設立研發中心、生產基地趨勢增強,高端研發人才往往被海外高薪與成熟商業化體系吸引。企業、人才、資本外流風險上升,產業鏈完整性會受到挑戰,關鍵時刻甚或影響國家醫藥產業安全。
進一步推動中國創新藥發展,當務之急是先把國內市場做起來,通過完善創新藥支付體系;推動各級政府、商業保險、慈善基金共同參與創新藥可及性專案,讓創新藥在國內「賣得動」;建設真實世界數據(RWD)平台,提升創新藥在國內的價值認定等,做強國內市場價值,形成「內外雙循環」的創新藥生態。同時加快創新藥在國內的審評審批與准入速度,推動創新藥在國內的臨床使用與醫療教育,才能真正把企業、人才與資本留住。
企業方面,未來應從「賣產品」轉向「建能力」,構建全球化研發、註冊、商業化三大能力體系。BD從追求「金額數量」轉向「合作品質」,從對外授權升級到共同開發與商業化( Co-Co)、融合了授權許可與股權交易的海外新公司(NewCo)、自主出海等模式。若能在行業層面聯手建設國際化臨床試驗與轉化醫學平台,推動「創新藥+醫藥研發生產外包服務組織(CXO)+供應鏈」形成組合整體出海,以及建立行業級地緣政治與合規風險資料庫,定能構建全球競爭力的創新生態。
國產創新藥認證 港大有可為
面對瞬息萬變的全球環境,也有必要在國家層面構建醫藥全球化的戰略安全體系。建立國家級醫藥全球化戰略協調機制,統籌海外註冊、全球臨床、知識產權保護、投資審查與地緣政治風險預警;加強產業鏈安全布局,支持國內建設高端原料藥、關鍵中間體和藥械國際化品質體系,防止關鍵環節外移。同時,積極參與全球公共衞生事務,加快加入藥品檢查合作計劃(PIC/S),深化與世衞組織(WHO)等機構溝通與合作,推動國際監管合作與標準互認,提升產品認受性和國家的話語權。
國產創新藥在出海過程中遭遇「准入難」,而作為連接中國與全球的「前沿港」,香港未來在推進國產創新藥認證方面可以發揮關鍵作用。如香港衞生署正申請成為WHO認可的藥物監管機構(WLA),若成功列名,將有助於加速新藥在港註冊,配合今年起分階段推行「第一層審批」新藥註冊機制,對支持中國創新藥出海具有重大意義。
(作者為創業投資者聯盟召集人)















 字號:
字號:


評論